过氧化氢酶活性测定方法 为什么淀粉遇到碘会形成蓝色化合物_今日聚焦
最近小编看到大家都在讨论过氧化氢酶活性测定(过氧化氢酶活性测定方法) 相关的事情,对此呢小编也是非常的感应兴趣,那么这件事究竟是怎么发生的呢?具体又是怎么回事呢?下面就是小编搜索到的关于过氧化氢酶活性测定(过氧化氢酶活性测定方法) 事件的相关信息,我们一起来看一下吧!
过氧化氢酶活性的测定(过氧化氢酶活性测定方法)
 (资料图片)
(资料图片)
原理:淀粉遇到碘,形成蓝色化合物。淀粉酶能把淀粉水解成麦芽糖,麦芽糖加碘后不会形成蓝色的化合物。
1.材料:新配制的淀粉酶溶液、鲜肝研磨液、可溶性淀粉溶液、双氧水溶液等。
2.步骤:
(1)探索温度对酶活性的影响。
温度对酶活性的影响
在温度对酶活性影响的实验中,除了温度外,三个试管的条件都是一样的。3号试管在60℃,酶活性更高,试管内淀粉分解,滴加碘溶液后不会变蓝。2号试管的温度条件是100℃,所以淀粉酶在高温下已经失去活性,1号试管的温度条件是O℃,在低温下抑制淀粉酶的活性。所以2号和1号试管中的淀粉还没有分解,滴加碘溶液后会变蓝,这个实验可以证明。酶的催化需要适宜的温度条件,温度过高或过低都会影响酶的活性。
(2)探索pH对酶活性的影响。
1实验过氧化氢(H2O2)在过氧化氢酶的催化下可以分解为水和氧气。可以用火星放入木条中,看是否可以重新点燃,检测是否产生氧气。
步骤试管1试管2试管3
1加入2mL2mL2mL过氧化氢溶液。
2加入1毫升蒸馏水—
加入3毫升盐酸溶液
加入氢氧化钠溶液——1毫升。
5滴肝研磨液,2滴,2滴
67℃水浴5min5min。
7检查
检查有火星的木条有无复燃现象。
试管内产生气泡:产生气泡,不产生气泡,不产生气泡。
2号试管加盐酸,溶液pH值低。3号试管加氢氧化钠,溶液pH值高。在pH过低或过高的环境中,过氧化氢酶失去活性,不能分解过氧化氢。没有氧气产生,但是没有酸或碱加入到1号试管中。溶液接近中性,过氧化氢酶将过氧化氢分解成水和氧气,导致木条复燃。
2实验
原理:淀粉在淀粉酶的作用下分解成麦芽糖,麦芽糖能与灼烧试剂发生氧化还原反应,生成砖红色沉淀。
步骤试管1试管2试管3
1加入2mL2mL2mL可溶性淀粉溶液。
2加入1毫升蒸馏水—
加入3毫升盐酸溶液
加入氢氧化钠溶液——1毫升。
5加入2滴2滴2滴新制备的淀粉酶溶液。
60℃水浴5min5min。
7加入2mL2mL2mL点火试剂。
80℃-60℃水浴2min2min2min。
9观测结果显示,有砖红色沉积物,无任何。
实验记录如下:1号试管有砖红色沉淀,2号试管无砖红色沉淀,3号试管无砖红色沉淀。
2号试管加盐酸,溶液pH值低。3号试管加氢氧化钠,溶液pH值高。在这样的pH环境下,淀粉酶失去活性,不能分解淀粉,所以试管中加入任斐林试剂后没有出现砖红色沉淀。1号试管中没有加入酸或碱,溶液接近中性。这样的pH值适合淀粉酶发挥催化作用,使淀粉分解并与灼烧试剂反应生成砖红色沉淀。以上实验可以证明,酶的催化作用需要合适的pH,pH过低或过高都会影响酶的活性。
例:①酶浓度对酶促反应的影响:当底物充足,其他条件固定,反应体系中不含抑制酶活性的物质和其他不利于酶发挥作用的因素时,酶促反应的速度与酶浓度成正比。
②底物浓度对酶促反应的影响:底物浓度较低时,反应速度随底物浓度的增加而加快,几乎与底物浓度成正比。底物浓度高时,反应速度加快,但不显著。当底物浓度较大并达到一定限度时,反应速率达到更大值。此时,即使底物浓度增加,反应也几乎不变。=。
③pH对酶促反应的影响:每种酶只能在一定的pH范围内显示活性,超过这个范围酶就会失去活性。其特点是曲线变化。在一定的条件下,每种酶在一定的pH值下活性更大,称为该酶的最适PH值。
④温度对酶促反应的影响:在一定温度范围内,酶促反应的反应速度随温度的升高而加快;但是,当温度升高到一定限度时,酶促反应的速率不仅停止加速,反而随着温度的升高而降低。在一定的条件下,每种酶在一定的温度下活性更大,称为该酶的最适温度。
\- 湖南旅游合同范本(热门3篇)
- 全球观点:云平台合同范本(10篇)
- 秘色瓷的秘是什么颜色 秘瓷的秘色指的其实是一种绿松石
- 特斯拉车顶维权女车主败诉 曾在前年大脑上海车展
- 世界观热点:【手慢无】锐龙6000系列笔记本限时特卖!
- 最新消息:李彦宏:未来50%的工作将是提示词工程
- 阿拉斯加雪撬犬 也被称为阿拉斯加的马拉穆 具有代表性 全球视讯
- 中国大学综合实力排行榜前200强 上海交大和武汉大学能排多少名 全球聚焦
- 15首经典轻音乐推荐 久石让的天空之城曾让无数人感动
- 阿迪达斯三叶草系列 这个款式已经逐渐演变成街头经典_资讯推荐
- 天天热点!洁具促销方案 怎样做才能更好的拿到订单 寻求解决方案?
- 该怎么保存网页:可以直接按组合键Ctrl+S保存网页吗_当前最新
- 世界今日报丨叉子用英语怎么说 复数怎么表达 希望可以给到大家一些参考
- 赠予合同范本单方(推荐12篇)
- 水杯订购合同范本(推荐3篇)|环球热推荐
- 天天观天下!心仪的商品还能再便宜吗?他们在这里找到了肯定答案
- 华为 P60 系列 618 优惠出炉,直降 800 到 1000 元-环球聚看点
- 火影忍者羁隐藏英雄密码 火影忍者羁绊6.52哪个隐藏英雄最厉害
- 赠予合同范本单方(推荐12篇) 世界快报
- 环球快资讯丨保护的反义词是什么 希望本文的总结能够对你有帮助
- 天天速读:河北定州属于哪个市 是河北省中部的中心城市 属河北省直辖市
- 最会画马的外国画家 郎世宁和中国历代画家画的马有着哪些区别
- 【天天新要闻】全新锐界汽车解析 福特全新锐界在福特杭州工厂生产吗
- 全球观天下!刀郎最经典演唱会盘点 曾经举行过十年环球巡回演唱会
- 现货黄金收盘时间 国际黄金的开盘和收盘时间是什么?
- 唐朝李怡在位几年 这是唐朝的第几位皇帝 生平如何
- 寂寞的近反义词是什么 希望能解答各位小伙伴的疑惑
- 面积计算器 面积是表示二维图形或形状或平面层在平面中的程度的量
- 天王山之战讲解 日本历史上最大、最著名的政变是什么
- 七月十五烧纸什么时候最好 各地的风俗习惯可能有所不同
- 免费物业合同范本(共11篇)
- 最全面的道路交通标志图解 红色交通标志就是代表禁止_世界今头条
- 安耐晒蓝瓶怎么样 最冷门的粉白瓶好用吗 7款安耐晒防晒讲解
- 金钗之年是多少岁 还有哪些词用来指代各个年龄段的女性-每日视讯
- 资讯:洛克王国电子超人超进化 获得洛克王国金钥匙的方式是什么
- 岳飞墓在哪个地方 岳飞之墓在杭州的西湖风景区 追谥武穆 速递
- 世界热消息:最全的火车座位分布图 坐火车的时候你喜欢坐在靠窗的位置上吗
- vr看房怎么制作 室内vr展示怎么做?全景效果图多少钱? 每日消息
- 齐刘海短发发型图片 小方脸的女生可以选择刘海整齐的短发发型-热文
- 台历定制合同范本(通用5篇)
- 啤酒工艺流程简述 啤酒生产大致可以分为三个主要过程_世界报资讯
- 广场拆除合同范本(优选13篇) 环球微头条
- PS展会各游戏播放量统计:《马拉松》超《蜘蛛侠2》
- 国风怪谈肉鸽策略卡牌新作《兰若异谭》5月26日正式登陆Steam_快播
- AI发展趋势预判,李彦宏称大模型即将改变世界 | 速途网
- 第五届汽车毫米波雷达/激光雷达大会6月苏州召开!精彩议程&参会名单抢先看!
- 索尼公布了 PS5 的 PlayStation VR2 销量和令人兴奋的游戏阵容 全球快消息
- 普元产品矩阵瞄定智能化升级,助推企业共赢万亿数字经济
- 当前观察:陆军棋怎么玩和摆放(陆军棋怎么玩)
- 机构:花生关注需求关注播种 暂时弱势震荡
- 李彦宏:百度很快会正式推出文心大模型3.5版本
- 东航C919首个商业飞行航班计划公布 独家焦点
- 今日播报!机构策略:股指将维持震荡格局 短期以观望为主
- 全球快报:清廉潜江建设|室组地联动破难题 严查群众身边腐败
- 618前,淘宝突然多了一大批不带货的直播间
- 世界快看:视频号6·18好物节大促即将上线,多项流量激励计划促进消费增长
- 湖北省天门市发布暴雨黄色预警
- 近500家世界一流供应商助力小鹏扶摇架构落地,引领高端智能电动汽车发展
- 至少的英文(至少的意思)
- 世界观速讯丨孔明灯的来历故事视频_孔明灯的来历
- 《心灵杀手2》黑人女主线索:或来自量子破碎彩蛋
- 绝不擦边的钢管舞表演 红毯扑街的动态图-天天看热讯
- 剁椒的做法最正宗的做法四川(剁椒的做法最正宗的做法) 环球聚焦
- 海南现震撼闪电犹如在夜空爬行 火蛇般照亮夜空
- 李彦宏:百度很快会正式推出文心大模型3.5版本
- 今日快讯:【手慢无】618热销爆款 华硕破晓2笔记本到手价3767元
- 【手慢无】限时抢购!OPPO Pad Air独家优惠仅1199元
- 老人沉迷网络跨越千里找男网红 非得见见他:网友感慨短视频害人 今日热议
- 马斯克:特斯拉可能像 Android 那样 向其他汽车制造商「开源更多代码」 天天即时
- 所有的飞机都有商务舱吗 所有的飞机都已经落了地是什么歌|热讯
- 六安白癜风到哪家医院好-出现在颜面部位的白癜风要怎样处理?
- 大明仙人小说排行榜 大明仙人
- 焦点热文:京津冀青龙湾森林半程马拉松日期及时间
- ps粉色参数 ps粉色数值
- 视焦点讯!2023京津冀青龙湾森林半程马拉松赛事信息
- 短讯!2023杭州各区小学学区划分汇总(更新中)
- 驾驶机动车在高速公路上行驶时 前轮爆胎时驾驶人控制住行驶方向后要采取什么措施减速停车_360_环球今日讯
- 全球观天下!网友被《蜘蛛侠复刻版》逼疯:画质模式频繁崩溃
- 火星异种ova完整版 火星异种ova
- 【环球新要闻】王者荣耀体验服爆料,打野骂骂咧咧,中单法师狂喜
- 宣传品有哪些东西 宣传品有哪些 世界球精选
- 2023京津冀青龙湾森林半程马拉松活动攻略
- 热消息:外媒锐评《魔戒:咕噜》:50美元?免费送都别玩
- 即时看!空调外机防护罩图片 空调外机防护罩
- 颠覆式洗衣机,深度清洁方案为家务做简法|每日快看
- 全球今亮点!向量共线定理公式 向量共线
- 【播资讯】2023浙江机场集团保安服务有限公司招聘通知
- 中国移动下架 17 款权益产品,这次影响人数较大 环球观点
- 2023年天津市北辰区幼儿园招生政策
- 京津冀青龙湾森林半程马拉松比赛项目|全球资讯
- 入驻2023数博会国际传播中心,华为擎云 G540辅助会务工作高效开展 世界速看料
- 【环球新视野】京津冀青龙湾森林半程马拉松比赛规模
- 世界播报:广州铁路局领导名单公示(广州铁路局)
- 每日讯息!蓝宝石RX 7600白金版OC显卡:2000元价位的高性价比游戏利器
- 热卖爆款游戏本 OMEN暗影精灵9 618闭眼入-最新消息
- 电脑屏幕闪烁颜色变化(电脑屏幕闪烁变色)
- 【手慢无】保价618!小米Book Air 13跌至4899元
- 焦点热文:卷轴屏iPhone要来了?苹果新柔性屏iPhone专利曝光
- 【手慢无】狂降700元!Apple iPad 9 2021款现价3099元!
- 光威天策内存条 618 再降新低:32GB 仅 299 元! 最新快讯
新闻排行
-
 关注:iCloud Drive是什么以及iCloud Drive是什么意思?
关注:iCloud Drive是什么以及iCloud Drive是什么意思? -
 【播资讯】红米6a和红米6买哪个好 红米6与红米6a区别对比详细评测
【播资讯】红米6a和红米6买哪个好 红米6与红米6a区别对比详细评测 -
 天天即时:OTA升级是什么意思
天天即时:OTA升级是什么意思 -
 环球焦点!下载App不再需要输入Apple ID的方法
环球焦点!下载App不再需要输入Apple ID的方法 -
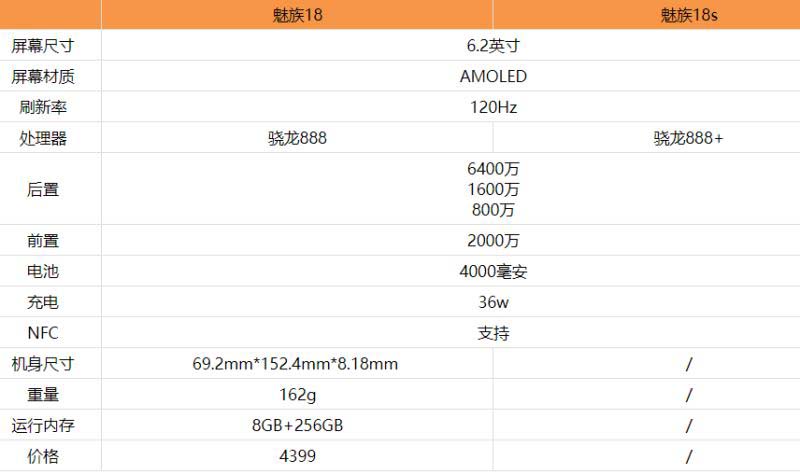 全球今亮点!魅族18s和魅族18区别是什么 魅族18s和魅族18对比评测
全球今亮点!魅族18s和魅族18区别是什么 魅族18s和魅族18对比评测 -
 天天热文:华为mate40和mate40pro哪个值得买?华为mate40对比mate40pro的区别
天天热文:华为mate40和mate40pro哪个值得买?华为mate40对比mate40pro的区别 -
 环球焦点!iPhone雷达功能怎么用?iPhone雷达功能(快播视频)查看教程
环球焦点!iPhone雷达功能怎么用?iPhone雷达功能(快播视频)查看教程 -
 环球信息:iphone手机用数据线连接电脑后只能充电无法进行文件传输的解决方法介绍
环球信息:iphone手机用数据线连接电脑后只能充电无法进行文件传输的解决方法介绍 -
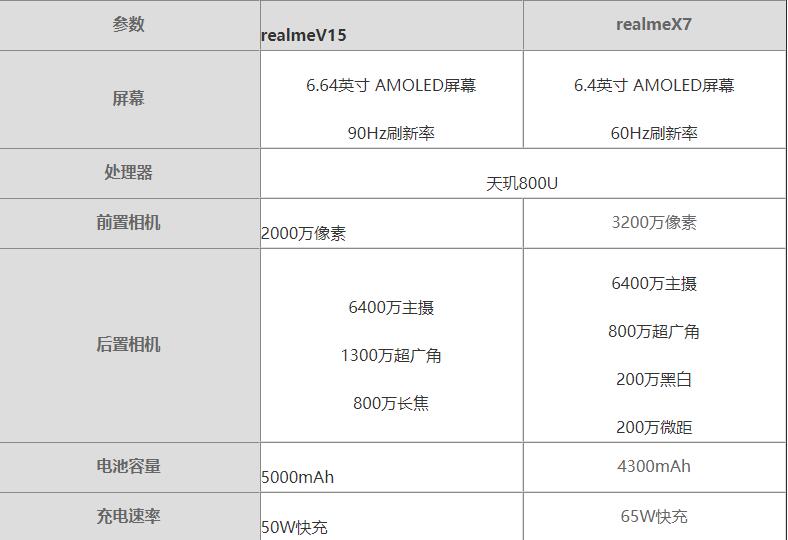 环球今热点:realmeV15对比realmeX7哪个好?realmeV15对比realmeX7评测
环球今热点:realmeV15对比realmeX7哪个好?realmeV15对比realmeX7评测 -
 当前视点!iOS 8.4 正式版发布 iOS 8.4到底升不升级?
当前视点!iOS 8.4 正式版发布 iOS 8.4到底升不升级?
精彩推荐
超前放送
- 北人生而不识菱者译文 它的寓意...
- 法拉第未来官宣:FF 91第一阶段...
- 豆油密度:大豆油是最常见的调味...
- 高校男生赤膊摆摊卖手打柠檬茶 ...
- 故宫北门叫什么名字 故宫的北门...
- 地下城双开怎么同步操作 TGP现...
- 考博要具备的条件是什么?今天小...
- 国家药品监督局官网查询_国家药...
- 焦点快看:哪个公式编辑器好用 ...
- 过氧化氢酶活性测定方法 为什么...
- 垫付协议_垫付
- 住房和城乡建设部干部学院培训专...
- 毕马威研究:生成式AI有望重塑工...
- 黑色幽默:是美国现代文学流派 ...
- 误会的英文单词有哪些 被误解的...
- 超级美洲豹直升机 山猫直升机是...
- 介绍推广近义词_介绍的近义词介...
- 当前时讯:丹渠两岸好“丰景”
- 聚焦:卡巴斯基激活码生成器 如...
- 冬天麦盖三层被来年枕着馒头睡的...
- 山青水绿山镇美如画
- 学会常见的配色原理,再也不怕后...
- nba球员薪水一览表 超过4000万...
- 有名经典的对子大全网罗总结 成...
- 安安洗面奶为什么便宜 说到佛山...
- 世界快资讯:【手慢无】华硕无畏...
- 猪心的做法大全来了 莲子猪心汤...
- 快讯:撞号是什么意思 小编将搜...
- 环球观速讯丨梦见掉头发 梦见梳...
- 火炬之光2狂战士加点:除了技巧之...
- 化妆品试用 是高效率的测试产品...
- 网上订购火车票流程 网上买火车...
- 终于等到!魅族20 INFINITY无界...
- 当前观察:abandon的梗_abandon这个梗
- 天天新动态:白日鼠白胜简介_白...
- 北风像什么怎么写比喻句 可以写...
- 君子莫大乎与人为善 只有善意才...
- 化学药品的取用与正确存放 取用...
- 人生如戏英文缩写 人生如戏全靠...
- 火车托运价格表 集装箱的运费是...
- 华为周斌:AI算力需求正快速增加...
- 一所学校学生会的会员 学生会的...
- 焦点关注:金鱼缸法则 圆形鱼缸...
- 全球今日报丨科普踩地神拔草龙 ...
- 体现汉字特点的古诗句 体现汉字...
- 怎么下载植物大战僵尸花园战争2_...
- 天天微头条丨寒雨连江夜入吴的下...
- 大理丽江香格里拉自由行攻略 你...
- 环球动态:高原反应包括睡不着觉...
- 钢琴属于什么乐器 从钢琴的结构...









